Retour à la bibliothèque Romer
8 mythes sur les tests de dépistage des agents pathogènes

Mythe 1
Les tests environnementaux de détection des pathogènes n'améliorent pas mon programme de sécurité alimentaire.
La plupart des réglementations relatives aux agents pathogènes exigent la réalisation de tests sur les produits finis avant qu'un lot de production alimentaire puisse être mis en circulation en toute sécurité pour la distribution et la vente au détail. Cependant, l'analyse des produits finis pose plusieurs problèmes. Tout d'abord, des variables telles que la microflore de fond, les caractéristiques inhibitrices, le niveau de pH et la concentration en sel rendent la détection des pathogènes difficile. Deuxièmement, les méthodes d'échantillonnage et l'hétérogénéité des échantillons peuvent entraîner des imprécisions, en particulier si les niveaux de contamination sont très faibles. Comment les producteurs de denrées alimentaires peuvent-ils être sûrs que le nombre d'échantillons testés est suffisant pour garantir que le lot est entièrement exempt de pathogènes dangereux ? Les analyses environnementales se sont révélées être un outil très utile dans de nombreux programmes de sécurité alimentaire et ont été adaptées dans le cadre des contrôles préventifs prévus par la loi de modernisation de la sécurité alimentaire (FSDA) de la FDA. Les programmes de surveillance de l'environnement (ou EMP) permettent à un producteur de denrées alimentaires de trouver des niches de croissance dans les zones de production et de prendre des mesures pour éliminer tout risque associé à la contamination des denrées alimentaires. Les zones présentant un risque élevé de contamination par des agents pathogènes doivent faire l'objet d'un échantillonnage, car l'objectif des tests environnementaux est de trouver des résultats positifs. L'objectif de la surveillance est d'éradiquer les agents pathogènes potentiels de l'installation et de la chaîne de production avant qu'une contamination réelle ne se produise, et de donner aux producteurs de denrées alimentaires une indication précoce de tout risque/problème de contamination.
Mythe 2
La recherche de pathogènes en interne nécessite des investissements substantiels
Les laboratoires de service disent souvent à leurs clients qu'il est trop coûteux et laborieux de tester les pathogènes alimentaires dans leurs propres installations. C'est peut-être vrai si des procédures standard (FDA BAM, ISO) sont utilisées, car elles nécessitent généralement beaucoup de temps de travail. D'autres méthodes, telles que l'ELISA et la PCR en temps réel, nécessitent un équipement coûteux. En fait, les seuls équipements dont vous avez besoin pour les tests internes sont un incubateur pour la phase d'enrichissement et une balance pour peser les échantillons. Un autoclave est facultatif, et uniquement si vous souhaitez stériliser vos propres milieux ou pour l'élimination des déchets. Il peut également être nécessaire de disposer d'une pièce séparée pour l'enrichissement et les tests. Lorsque vous utilisez des bandelettes à flux latéral, vous n'avez pas besoin d'équipement supplémentaire pour interpréter les résultats et, par conséquent, aucun investissement substantiel n'est nécessaire.
Mythe 3
Le dépistage des agents pathogènes nécessite un personnel bien formé
Les méthodes rapides de détection des agents pathogènes ont été rationalisées par rapport à l'époque où seuls des microbiologistes hautement qualifiés pouvaient effectuer ces tests, avec d'innombrables tubes et plaques et un œil avisé. Diverses compétences sont encore requises, en fonction de la méthode, mais de nombreux kits de test peuvent être utilisés efficacement par du personnel formé. Toutes les méthodes de test n'exigent pas un personnel hautement qualifié. Dans de nombreuses entreprises, le personnel de laboratoire peut avoir été transféré de l'usine de production et ne pas avoir de diplôme scientifique. Les méthodes d'essai doivent donc être simples et robustes, avec un minimum d'étapes pour aider à rationaliser le flux de travail dans le laboratoire et minimiser le risque d'erreurs. Un laboratoire doit également être en mesure de prouver que son personnel a été formé à la méthode d'essai en vigueur. Certaines entreprises participent également à des programmes d'essais d'aptitude afin de s'assurer que leur personnel de laboratoire peut travailler de manière indépendante et obtenir des résultats d'essais précis.
Mythe n° 4
Les exigences en matière de sécurité des laboratoires dissuadent les petites entreprises d'effectuer leurs propres tests.
Les agents pathogènes alimentaires du groupe de risque 2, tels que Salmonella, Listeria et E.coli O157, peuvent être manipulés dans des locaux moyennant quelques ajustements mineurs. Les agents pathogènes de ce groupe de risque ne sont pas considérés comme dangereux pour les travailleurs de laboratoire et la communauté en général. Selon la norme européenne EN 12128, Biosafety in Microbiological and Biomedical Laboratories (US Centers for Disease Control and Prevention) et le manuel de biosécurité de l'Organisation mondiale de la santé (OMS), ces salles doivent être marquées du symbole de danger biologique et leur accès doit être limité. Seules les personnes travaillant avec les agents pathogènes doivent avoir accès à cette salle de laboratoire. Les surfaces de la salle doivent être résistantes aux produits chimiques et donc aux désinfectants. Ces exigences en matière de sécurité des laboratoires peuvent être facilement gérées par les petits producteurs de denrées alimentaires.
Mythe 5
Je ne peux pas me débarrasser du matériel d'essai contaminé.
Oui, vous pouvez le faire. Voici trois options pour l'éliminer en toute sécurité : 1. Utilisez un autoclave et réglez la température à 121°C pendant au moins 20 minutes. Le matériel peut alors être éliminé en toute sécurité en tant que déchet résiduel. 2. Utilisez un système de désinfection par micro-ondes. Le matériel peut maintenant être éliminé en toute sécurité en tant que déchet résiduel. 3. Confiez cette tâche à une entreprise de gestion des déchets. Elle commandera des conteneurs spéciaux pour collecter les déchets contaminés et les éliminer pour vous.
Publié le :
Microbiologie

Mythe 6
Il n'est pas nécessaire de poursuivre l'analyse des échantillons après un résultat positif.
Toutes les méthodes rapides disponibles dans le commerce sont des tests de dépistage et nécessitent une confirmation culturelle après un résultat "présumé positif". La confirmation nécessite l'ensemencement de la portion de test enrichie sur des géloses sélectives afin d'isoler une colonie typique sur la base de ses caractéristiques morphologiques et biochimiques. Ceci est particulièrement vrai lors de l'analyse de produits finis ou de denrées alimentaires. Pour les échantillons environnementaux, la confirmation culturelle est rarement effectuée car des pratiques d'assainissement supplémentaires sont souvent mises en place. Il existe plusieurs options pour les géloses sélectives, les plus courantes se trouvant dans le Microbiology Laboratory Guidebook (MLG) de l'USDA, le Bacteriological Analytical Manual (BAM) de la FDA ou les guides de référence de l'ISO (voir tableau 1).

Mythe 7
Il n'y a aucune raison de tester les espèces de Listeria lorsque L. monocytogenes est l'adultérant.
Listeria monocytogenes (L'mono) est peut-être la seule souche de Listeria réglementée, mais elle n'est pas la seule pathogène. Listeria ivanovii est une autre souche pathogène susceptible d'être présente dans votre établissement. Une autre raison de tester les Listeria spp. (toutes les souches de Listeria), en particulier dans l'environnement de transformation, est de suivre les niches de croissance. En effet, L'mono peut potentiellement se développer là où d'autres souches de Listeria prospèrent. La présence ou non de L'mono est une question de probabilité. Si de nombreuses souches de Listeria non pathogènes (telles que Listeria innocua) sont présentes dans un échantillon, elles peuvent "surproduire" L'mono dans le processus d'enrichissement et potentiellement provoquer un résultat faussement négatif. Il n'est pas possible de cultiver une seule espèce de Listeria (c'est-à-dire L'mono) pendant l'enrichissement sélectif.
Mythe 8
Toutes les méthodes disponibles dans le commerce sont identiques
Il existe aujourd'hui une pléthore de méthodes rapides sur le marché et le choix entre elles peut être décourageant. Comment un producteur de denrées alimentaires peut-il déterminer la méthode qui lui convient le mieux ? Toutes les méthodes rapides disponibles dans le commerce se composent de deux parties : une étape d'enrichissement suivie d'une étape de détection. Différents milieux sont utilisés au cours de la phase d'enrichissement, soit un bouillon conventionnel, soit un bouillon propriétaire. La principale différence réside dans l'étape de détection. Les méthodes immunologiques détectent les protéines, tandis que les méthodes PCR détectent l'ADN. Les critères d'évaluation suivants doivent être pris en compte : inclusivité, exclusivité, sensibilité, spécificité, limite de détection, reproductibilité, répétabilité et certification (voir tableau 2).
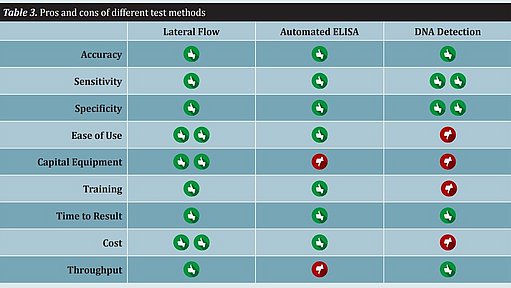
Les méthodes rapides diffèrent considérablement en ce qui concerne le flux de travail, la facilité d'utilisation et le débit. Plusieurs autres caractéristiques d'une méthode d'essai doivent être prises en compte, notamment les dépenses d'équipement, la formation, le délai d'obtention des résultats et le coût. Toutes ces caractéristiques doivent être prises en considération lors de la mise en œuvre d'une méthode rapide. Il n'existe pas de méthode unique qui convienne à tous les producteurs de denrées alimentaires (voir tableau 3).